将活体生物系统作为材料合成平台,已成为功能性纳米复合材料研究的一个重要方向。相比传统的体外合成方法,细胞内原位构建材料具有环境友好、反应温和、空间控制精确等优势。因此,如何有效调动细胞这一“天然反应器”的功能,引导其在体内合成复杂纳米结构,成为当前亟需攻克的关键技术难题。
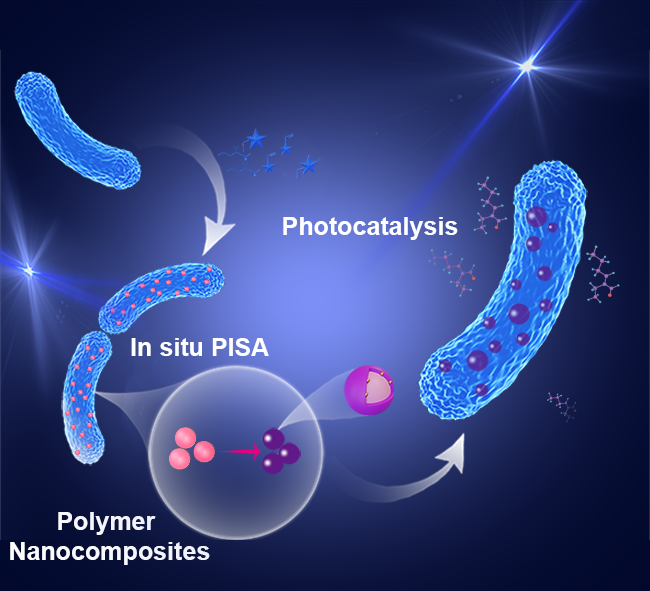
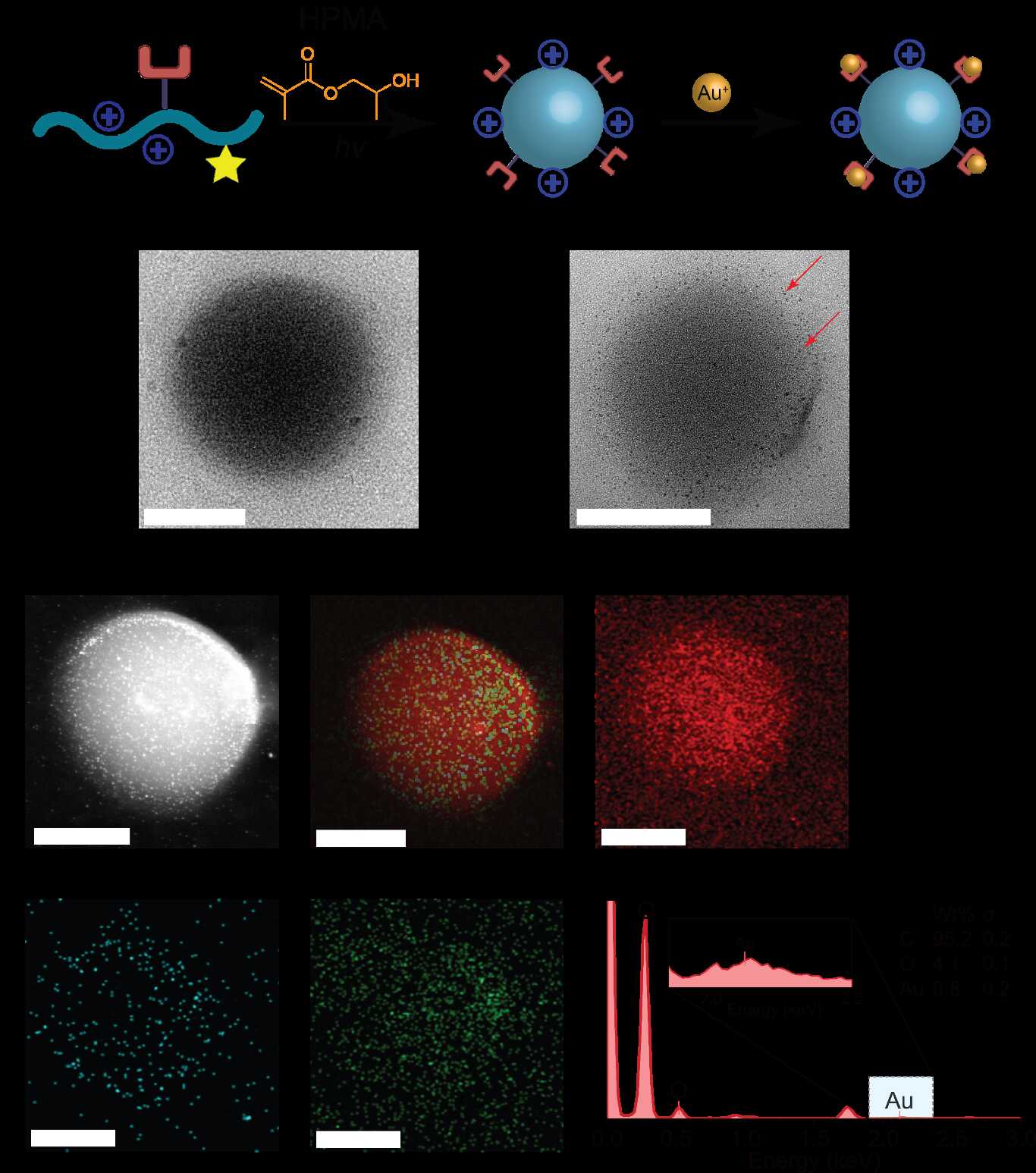
近期,中国科学院深圳先进技术研究院耿晋研究员团队在Angewandte Chemie International Edition上发表研究论文,题为“Intracellular Polymerization Induced Self-Assembly and Gold Nanocomposite Synthesis in Living Bacteria”。该工作发展了一种基于细胞内聚合诱导自组装(iPISA)的新策略,实现了在活大肠杆菌中合成金–聚合物纳米复合物,将细菌转化为“活体纳米制造工厂”。
细胞内自组装的设计与调控
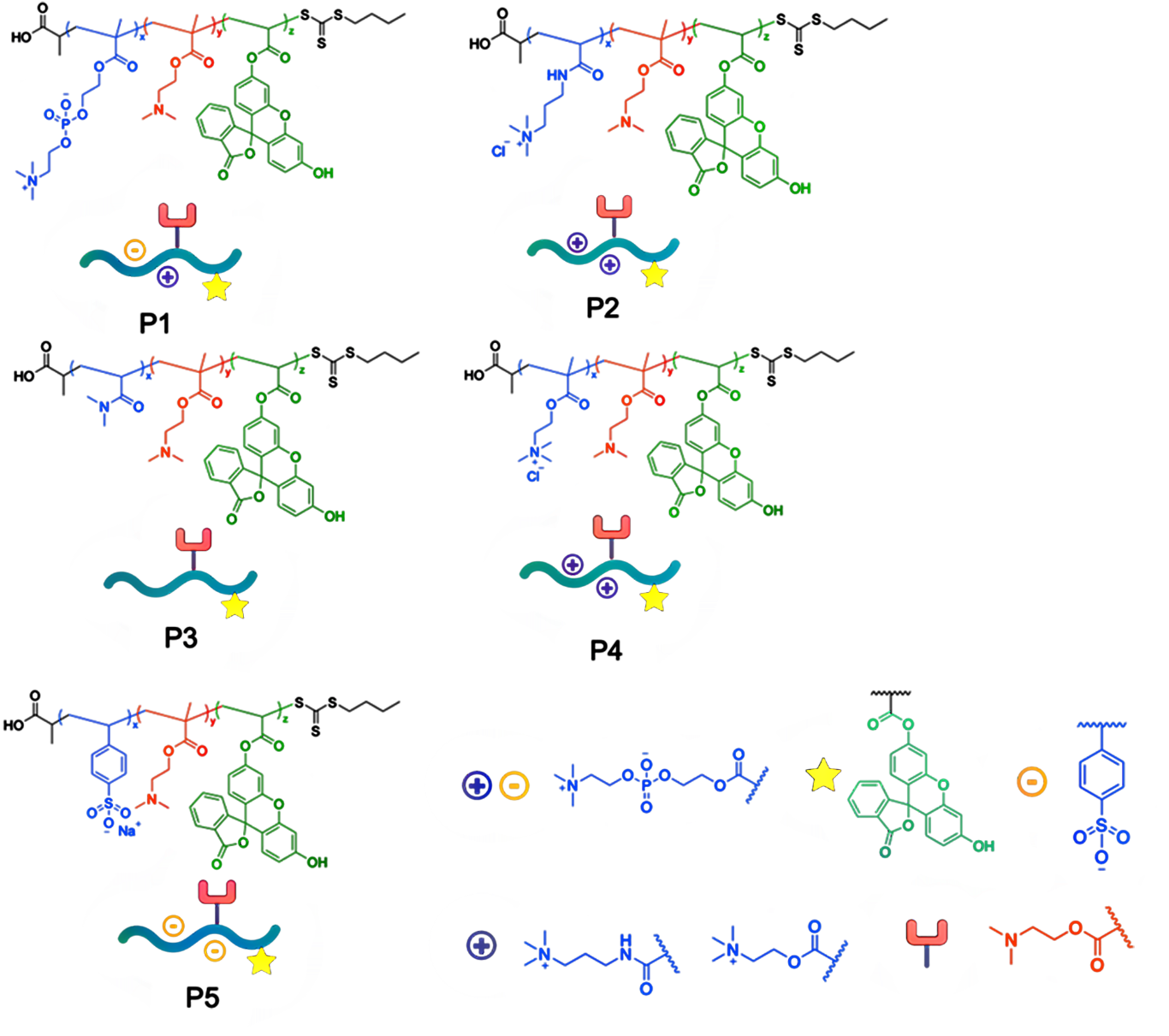
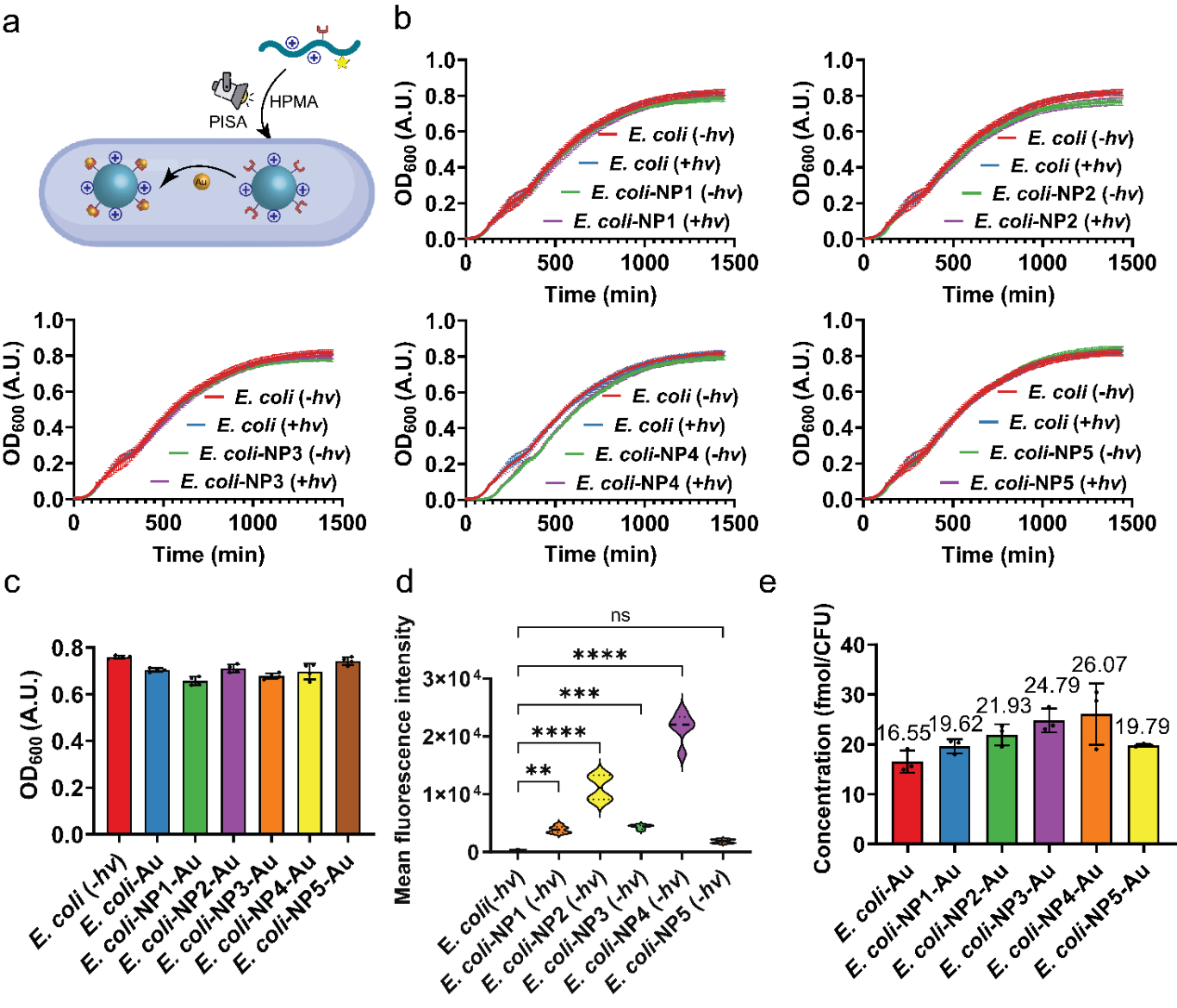
研究团队设计了一系列结构和电荷性质不同的聚合单体,通过RAFT聚合机制在细胞内引发自组装。结果发现,不同电荷特性的聚合物与细胞膜的相互作用差异显著,直接影响材料的空间分布。某些配方更倾向于在细胞内部形成纳米复合物,而另一些则主要定位于细胞表面。这一结果为调控纳米材料的合成位置提供了可行策略:只需调整反应体系中的关键成分,即可实现在胞内或胞外构筑功能材料。
拓展功能:构建细菌-材料杂合体系用于光催化反应
除了材料合成,该体系在功能拓展方面也表现出良好潜力。团队进一步利用“负载”金-聚合物复合材料的大肠杆菌,开展了光催化反应研究。结果表明,这些“杂合细菌”能够在温和条件下催化醛醇缩合反应,有效合成2-乙基己烯醛。此外,复合材料中的金纳米颗粒可吸收可见光,激发高能电子,从而提升聚合物材料的光催化活性。在染料罗丹明B的降解实验中,该体系亦表现出优异效率,显示出在环境治理领域的应用潜力。
展望与意义
本研究展示了活细菌在纳米复合材料原位构建中的独特优势,为绿色合成提供了新策略。通过精确调控细胞内外的反应行为,该方法有望在催化、传感、生物制造等领域实现更广泛应用。
该工作由中国科学院深圳先进技术研究院耿晋研究员、戴卓君研究员和澳门大学郭珩辉研究员共同通讯,博士研究生张诗玲为第一作者。研究获得国家自然科学基金、国家重点研发计划、广东省珠江人才计划以及深圳市医学研究专项等资助支持。

附件下载:


